Ce que nous avons appris en mettant sur pied la Cohorte de référence — et comment cela façonne la Phase 2 du Réseau des centres d'oncologie du Marathon de l'espoir

Par le Dr Jim Woodgett, président et directeur scientifique de l’Institut de recherche Terry Fox, et le Dr André Veillette, directeur général du Réseau des centres d'oncologie du Marathon de l'espoir
En 2019, le gouvernement du Canada a réalisé un investissement historique visant à accélérer les progrès en oncologie de précision et à transformer la manière dont le cancer est étudié et traité partout au pays. Cet investissement a permis de lancer la Phase 1 du Réseau des centres d'oncologie du Marathon de l'espoir (MOHCCN), une initiative pan-canadienne ambitieuse dirigée par l’Institut de recherche Terry Fox et la Fondation Terry Fox.
Dès le départ, notre ambition était claire : rassembler les milieux de la recherche sur le cancer et les milieux cliniques du Canada autour d’une vision commune et élaborer ensemble une stratégie nationale visant à accélérer la recherche en oncologie de précision et à la rendre accessible à un plus grand nombre de patients, quel que soit leur lieu de résidence.
Cinq ans plus tard, cette vision s’est concrétisée.
Plus de 1 300 collaborateurs issus de 54 établissements et plus de 100 partenaires se sont unis pour mettre en place une initiative véritablement nationale. Parmi ses réalisations les plus marquantes figure la création de la Cohorte de référence du MOHCCN, la base de données sur les cas de cancer la plus vaste et la plus complète du Canada, qui intègre les données cliniques et génomiques de plus de 15 000 patients.
Il s’agit d’un atout fondamental pour le pays, mais sa mise en place n’a pas été sans difficulté.
Alors que nous achevons la Phase 1, il est utile de réfléchir aux leçons tirées au cours des cinq dernières années et à la manière dont elles orientent notre approche de la Phase 2 du Réseau.
La mise en place d’un réseau national demande du temps… et de la confiance
Bien que le financement du Réseau ait été annoncé au début de 2019, les activités ont officiellement démarré à la mi-2021, à la suite de la signature d’une entente de contribution avec Santé Canada. Ces années intermédiaires ont été marquées par la pandémie de COVID-19, qui a perturbé la recherche, retardé les activités et mis à rude épreuve les établissements partout au pays.
Malgré la longueur de ce processus, les travaux n’ont pas marqué le pas. Les chercheurs, les cliniciens et les dirigeants ont continué à se réunir, à planifier et à harmoniser leurs priorités. Au moment du lancement officiel du Réseau, une feuille de route commune était déjà en place.
Même alors, les premiers progrès ont été plus lents que prévu.
Avec le recul, cela n’aurait pas dû être une surprise. Le Canada n’avait jamais tenté d’harmoniser la collecte de données génomiques et cliniques entre les établissements à une telle échelle. Chaque centre disposait de ses propres infrastructures, de ses propres processus et de son propre niveau de préparation. La mise en place d’un système unifié exigeait non seulement une harmonisation technique, mais aussi une relation de confiance entre les chercheurs, les oncologues et les administrateurs, qui travaillaient tous dans des établissements différents et étaient soumis à des réglementations différentes.
La mise sur pied de groupes de travail composés d’experts de partout au pays s’est avérée essentielle pour instaurer la confiance et surmonter ces défis. Ces groupes ont élaboré des politiques, défini des normes et – ce qui est peut-être le plus important – contribué à aplanir les différences dans les pratiques. En partageant nos connaissances, notre expérience et nos ressources, nous avons pu mettre en place une plateforme collaborative où les grands centres ont apporté leur soutien aux plus petits et où des capacités ont été développées à l’échelle nationale.
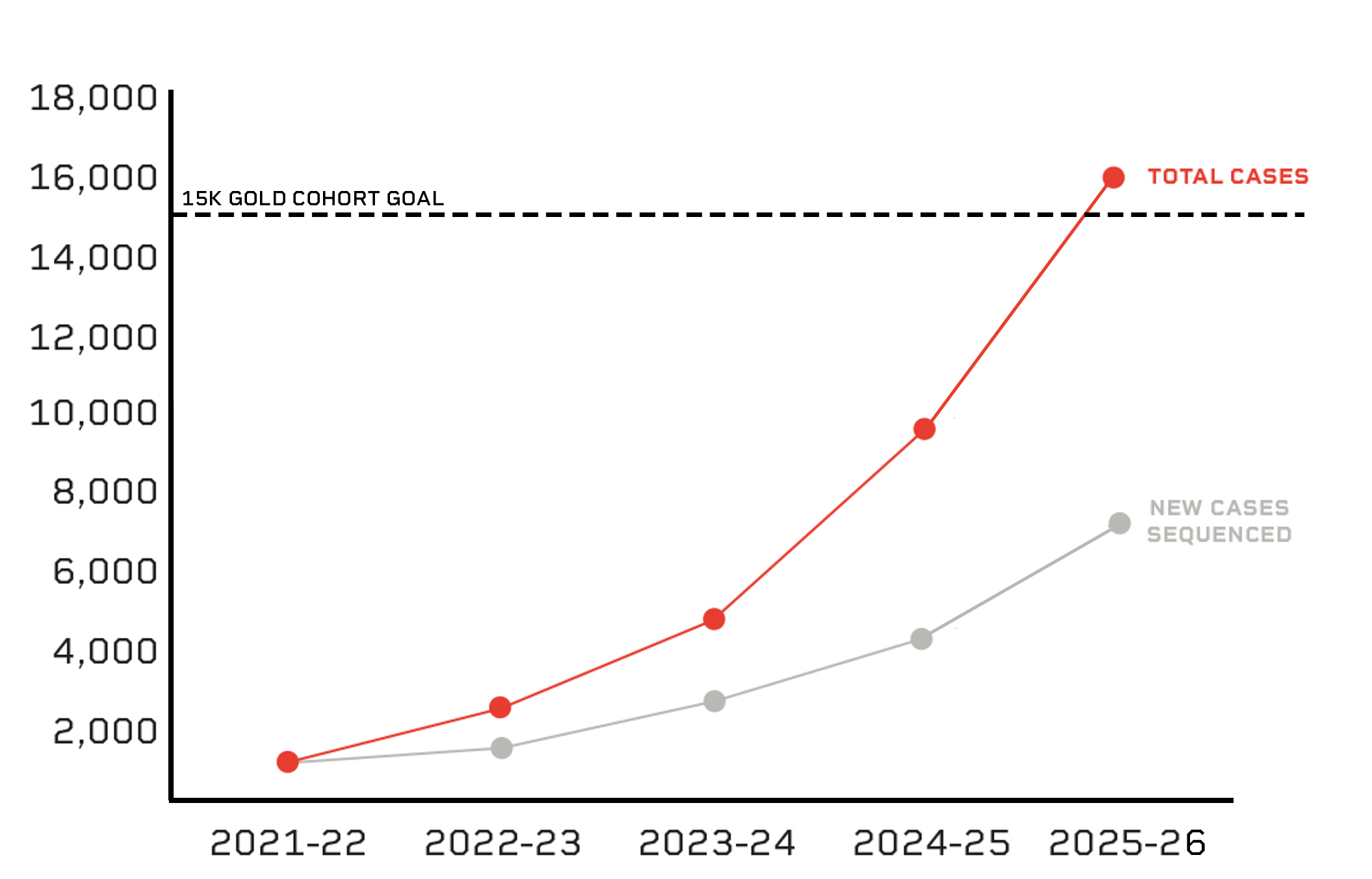
L'impact de ce modèle collaboratif et du cadre qu'il a contribué à mettre en place s'est clairement manifesté au fil du temps. Après des débuts timides, la production de données s'est considérablement accélérée, le nombre de cas ayant fait l'objet d'un profil complet ayant presque doublé d'une année à l'autre. Ce qui n'était au départ qu'un défi de coordination complexe s'est transformé en un système national évolutif.
Données cliniques : essentielles, complexes et exigeantes en ressources
L’un des principaux atouts de la Cohorte de référence réside dans le fait que chaque cas de cette base de données comprend des données cliniques soigneusement annotées, associées aux données génomiques. Cela permettra aux chercheurs d’étudier comment les caractéristiques génomiques influencent des aspects tels que le diagnostic, la réponse au traitement, l’évolution de la maladie et l’issue clinique des patients — des informations indispensables pour traduire les connaissances moléculaires en améliorations concrètes des soins aux patients.
Mais si la production de données génomiques à grande échelle à travers le pays posait des défis techniques, les données cliniques ont révélé une complexité d’un autre ordre.
La collecte des antécédents thérapeutiques, des résultats et des parcours des patients exige du temps, de l’expertise et une validation minutieuse. C’est particulièrement vrai dans un environnement de soins de santé fédéré comme celui du Canada, où les systèmes de santé ne recueillent pas les données cliniques de manière uniforme. Surmonter ces défis a demandé du temps et de nombreuses discussions, mais un modèle de données cliniques normalisé a finalement été créé, permettant aux centres de tout le pays de mettre en œuvre des protocoles de gestion des données adaptés à leurs propres systèmes, ce qui a permis de recueillir des données normalisées à l’échelle nationale.
L'élaboration de ces protocoles a pris du temps, ce qui a entraîné un décalage entre la collecte des données cliniques et celle des données génomiques. Ce décalage était, du moins en partie, voulu. En effet, les centres s'assurent généralement que les données génomiques répondent aux normes de qualité avant de se lancer dans l'annotation clinique. De plus, les données cliniques pertinentes dépendent souvent d'événements qui surviennent après le prélèvement des échantillons, comme la réponse au traitement.
Ce processus a permis de tirer une leçon claire : les données cliniques de haute qualité sont à la fois indispensables et exigeantes en ressources, c’est-à-dire qu’elles nécessitent beaucoup d’efforts et de temps.
La Phase 1 a mis en évidence la nécessité d’explorer de nouvelles approches, notamment l’automatisation partielle de l’extraction et du traitement des données. À l’aube de la Phase 2, il sera essentiel d’améliorer l’efficacité et l’évolutivité de l’ingestion des données cliniques pour maximiser la valeur de la Cohorte de référence, ainsi que de réduire les coûts de ces processus.
La flexibilité, une nécessité
Cela nous amène à l’un des enseignements les plus importants que nous avons tirés de la Phase 1 : la flexibilité est essentielle pour fonctionner à grande échelle.
La Cohorte de référence a été conçue selon des normes rigoureuses, mais l’application de ces normes dans des contextes concrets a nécessité une adaptation réfléchie. Un exemple frappant est apparu au cours de l’« Année de l’accélération des données » du Réseau, en 2023–2024.
De nombreux centres ont signalé des cas où le séquençage du génome entier (ADN) s’est avéré concluant, mais où le séquençage du transcriptome (ARN) n’a pas satisfait aux critères de qualité, en particulier pour les échantillons conservés en biobanque, où la dégradation de l’ARN est fréquente. Le maintien d’exigences strictes pour ces deux types de données aurait conduit à l’exclusion de données précieuses.
La solution a consisté à faire évoluer la définition d’un cas de la Cohorte de référence. Les cas de niveau A comprennent à la fois le profilage de l’ADN et de l’ARN, tandis que les cas de niveau B comprennent uniquement des données d’ADN. Cet ajustement a permis de préserver la qualité des données tout en élargissant l’utilité de l’ensemble de données. Aujourd’hui, environ 85 % des cas comprennent les deux types de données.
Ce principe s’étend au-delà de la génomique elle-même.
Les modèles de données cliniques, par exemple, se sont révélés plus difficiles à normaliser pour l’ensemble des types de cancer. Les cancers du sang, en particulier, présentent des caractéristiques propres qui ne correspondent pas toujours aux cadres applicables aux tumeurs solides. Plutôt que d’imposer une uniformité, le Réseau s’est adapté, en affinant les champs de données et en planifiant de nouvelles améliorations pour la Phase 2.
Dans ce contexte, la flexibilité ne consiste pas à abaisser les normes. Il s’agit plutôt de veiller à ce que les normes demeurent pertinentes, inclusives et scientifiquement significatives.
La représentativité est essentielle
Au-delà de la qualité des données, l’un des principaux objectifs du Réseau était de créer une base de données qui reflète la diversité de la population canadienne et qui permette de faire progresser l’oncologie de précision au profit de tous les patients, et pas uniquement de ceux généralement représentés dans ce type de recherche.
La Phase 1 a permis de réaliser des progrès importants dans ce sens. Le Réseau s’est étendu à l’ensemble des dix provinces en seulement trois ans, réunissant ainsi des établissements d’un océan à l’autre. Le Groupe de travail sur le cadre canadien a également établi des lignes directrices visant à identifier les communautés mal desservies et les populations sous-représentées dans la recherche sur le cancer.
Cependant, il est clair qu’il subsiste d’importantes lacunes.
La participation des Territoires a été limitée, et la représentation de certains groupes – notamment les communautés des Premières Nations, des Inuits et des Métis – n’a probablement pas répondu aux attentes démographiques. Dans de nombreux cas, cette situation a été aggravée par le manque de données sociodémographiques cohérentes, ce qui rend difficile de déterminer avec précision dans quelle mesure la Cohorte de référence est réellement représentative de l’ensemble des diverses populations du Canada.
Il s’agit là d’un domaine où des améliorations s’imposent absolument.
La Phase 2 prévoit une initiative concertée visant à étendre les activités aux régions rurales, éloignées et nordiques, ainsi qu’à renforcer les partenariats avec les communautés mal desservies. La mise au point d’un nouveau modèle de données sociodémographiques favorisera également une collecte de données plus éthique, plus cohérente et plus pertinente, contribuant ainsi à une répartition plus équitable des bénéfices de l’oncologie de précision.
Des bases solides pour s'adapter aux défis futurs
La recherche scientifique se déroule rarement exactement comme prévu. Les technologies évoluent, les connaissances progressent et de nouvelles questions apparaissent.
C’est pourquoi le Réseau est resté ouvert à l’exploration de nouvelles technologies de profilage pouvant être intégrées à la Cohorte de référence du MOHCCN lors des phases futures du Réseau. L’exploration de ces nouvelles technologies, soutenue par les bourses de développement technologique de l’IRTF-MOHCCN, fournit des informations précieuses qui nous aideront à accroître le potentiel d’impact de la Cohorte de référence lors de la Phase 2 et à maintenir le Réseau à l’avant-garde de l’innovation.
Bien que nous nous soyons constamment adaptés à la réalité sur le terrain et que nous ayons exploré de nouvelles technologies de profilage pour obtenir une image plus complète du cancer, l’un des aspects les plus frappants du MOHCCN réside dans la façon dont il est resté fidèle à sa vision initiale. Les principes fondamentaux établis dès le départ – collaboration, excellence, coordination nationale et impact sur les patients – ont perduré, tout comme notre capacité à accroître le potentiel d’impact de la Cohorte de référence du MOHCCN.
Ce n’est pas le fruit du hasard.
Ces principes ont été élaborés à la suite d’une vaste consultation, s’appuyant sur l’expérience internationale et affinés en permanence grâce aux contributions d’experts issus du Réseau et d’ailleurs. Ces bases solides ont permis au Réseau de s’adapter sur le plan opérationnel sans perdre de vue ses objectifs.
Regard vers l’avenir
Depuis le lancement officiel de nos activités en 2021, nous avons :
Réuni plus de 1 300 patients, chercheurs, cliniciens, administrateurs et donateurs issus de plus de 100 établissements à travers le pays pour former l’Équipe Canada de la recherche sur le cancer...
Créé la ressource de cas de cancer la plus importante et la plus complète au Canada...
Financé des recherches sur le cancer ayant un impact significatif partout au pays...
Renforcé les capacités en ressources humaines du Canada en matière de cliniciens-chercheurs, d’informaticiens de la santé et de scientifiques des données...
Donné davantage de poids à la voix des patients dans la recherche...
Et contribué à rendre l’oncologie de précision accessible à un plus grand nombre de Canadiens !
Le Réseau étant désormais solidement établi, l’accent sera mis sur l’élargissement de son champ d’action et de sa portée : il s’agira d’atteindre davantage de patients et d’intégrer plus profondément l’analyse génomique aux soins cliniques, de manière efficace tant sur le plan des coûts que du temps. Tout aussi important, cela permettra de tester les performances de cette infrastructure dans des conditions réelles, où son impact sur les résultats pour les patients pourra être pleinement mis en évidence. Cela témoigne des efforts extraordinaires déployés par une communauté nationale unie par un objectif commun. Plus important encore, cela jette les bases de la prochaine phase de découverte, d’innovation et d’impact.
Si la Phase 1 visait à mettre en place le système, la Phase 2 consiste à le tester — à grande échelle, à travers le pays et au bénéfice de tous les Canadiens.
Alors que nous arrivons au terme de la Phase 1, il est utile de réfléchir aux leçons tirées au cours des cinq dernières années et à la manière dont elles influencent notre approche de la Phase 2 du Réseau.
Personnes apparentées
-
Jim
Conseil du RéseauSiège social et opérationsMembre de groupe de travail
Woodgett -
André
Executive Director
Veillette
